| 独立行政法人 理化学研究所 神戸研究所 発生・再生科学総合研究センター |
2011年11月14日 |
ES細胞やiPS細胞から組織や臓器はつくれるのだろうか。発生中の生体内の環境を培養条件に反映させることで、これらの幹細胞から様々な種類の細胞を分化させる研究が進んでいる。しかし、立体的な組織や臓器は複雑な組織間の相互作用を経て形成されるため、これを試験管内で再現することは容易でない。一方、ES細胞は特定の条件下で生体内と良く似た組織構造を形成しうることが報告され、細胞間の相互作用の結果によりパターンが自然に生じる「自己組織化」と呼ばれる概念がそのメカニズムとして注目されている。 理研CDBの須賀英隆研究員(立体組織形成・解析ユニット)と笹井芳樹グループディレクター(器官発生研究グループ)らは、マウスES細胞から機能的な下垂体組織を試験管内で形成することに初めて成功した。この研究は名古屋大学大学院医学系研究科の大磯ユタカ教授との共同で行われ、イギリスの科学誌Natureに11月9日付けでオンライン先行発表された。
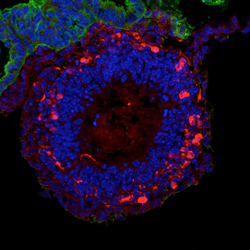
同グループはこれまでに、ES細胞から神経系の細胞を効率よく分化させる「無血清凝集浮遊培養法(SFEBq)」を開発し、中脳ドーパミン神経細胞、大脳神経細胞、小脳プルキンエ細胞などの誘導に成功している。近年ではこの培養法を応用し、生体内と同様の層構造をもつ大脳皮質や網膜の組織を試験管内で構築することにも成功していた。 今回、須賀研究員は、SFEBq法を応用してES細胞からの下垂体組織の形成に挑んだ。間脳の視床下部にぶら下がる下垂体は、ホルモン分泌の制御中枢として知られ、全身の恒常性維持に極めて重要な働きをもつ。下垂体(腺性下垂体)は発生学的には口腔外胚葉に由来する。視床下部の前駆組織が隣接する口腔外胚葉に働きかけ、その一部が陥入して袋状のラトケ嚢となる。ラトケ嚢はやがて下垂体へと成熟し、視床下部の制御を受けて様々な制御ホルモンを血中に分泌する。 同グループは過去の研究で、SFEBq法の培養液から血清や増殖因子を取り除くと、視床下部細胞が誘導されることを示していた。今回、条件検討の結果、SFEBq法で立体培養をする際に、約1万個のES細胞を用いてより大きな細胞塊を形成すると、視床下部細胞と口腔外胚葉細胞が共に誘導されることを見出した。これらの細胞は一つの凝集塊の中で混在すること無く、生体内の状態と同様に2つの層を形成していた。詳しく調べると、細胞塊が大きくなることでBMPシグナルが増強され、それが口腔外胚葉細胞の分化を導いているようだった。 そこで、このラトケ嚢をさらに培養し、内分泌機能をもつ成熟した下垂体を形成できるかどうかを検証した。まず、下垂体が分泌するホルモンのなかでも特に個体の生存や活動性の維持に重要な副腎皮質刺激ホルモン(ACTH)に着目した。NotchシグナルがACTH産生細胞の分化を阻害することが報告されていたため、Notchシグナルの阻害剤を添加して培養したところ、ラトケ嚢からACTH産生細胞が高頻度に分化した。また、Wntシグナル、糖質コルチコイド、インスリンの存在下では、成長ホルモン産生細胞の分化も確認された。また、分化効率は下がるものの、培養条件を調節することで他の下垂体ホルモン産生細胞も誘導できることがわかった。ACTH産生細胞についてさらに詳しく調べると、ACTHを産生するだけでなく、生体内と同様に、副腎皮質刺激ホルモン放出ホルモン(CRH)による正の分泌制御や、副腎皮質ホルモン(ACTHの下流ホルモンで、副腎が産生する)による負の分泌フィードバックを受けることが明らかになった。
彼らは最後に、ES細胞由来の下垂体をマウスに移植する実験を行った。成体マウスの下垂体を除去して下垂体機能不全マウスをつくり、ACTH産生細胞を含むES細胞由来下垂体を腎臓の被膜下に移植した。すると、移植1週間後には、移植しなかったマウスに比べて有意に血中のACTH濃度が上昇し、さらにCRHの注射に応答してACTH濃度が正常値近くまで回復することがわかった。これに伴い、血中の副腎皮質ホルモンの濃度も上昇していた。また、下垂体機能不全マウスでは自発的な活動性が低下し、8週間以内に全てが死亡したが、下垂体を移植したマウスでは活動量が回復し、移植後8週間の生存率が85%強にまで上昇することが示された。 今回の研究結果は、ES細胞が高い自己組織化能をもち、場合によっては複数の組織の相互作用を必要とする器官形成すら可能であることを示している。器官の形づくりのプログラムがどこまで細胞自身に書込まれているのかについて、驚くべき自律性の存在を明らかにしたと言える。笹井芳樹グループディレクターは、「立体培養による自己組織化が、以前の研究で示された神経系や感覚系器官だけでなく、今回、内分泌器官といったより幅広い器官の構築原理として働くことが明らかになりました」と話す。今回の成果は医学応用面での意義も極めて大きい。自身が内分泌内科医である須賀研究員は、「下垂体の機能不全に対しては、不足しているホルモンを投与する補填療法が行われていますが、量的変動の大きいホルモンを適切に補填するのは容易ではありません。これまで現実的とされていなかった内分泌系の再生医療の基盤を築いて行きたいと思います」。
|
|||||||||||||||
 |
| Copyright (C) CENTER FOR DEVELOPMENTAL BIOLOGY All rights reserved. |